Baseinas / baseinas / „Getty Images“
Pagrindiniai išsinešimai
- FDA suteikė leidimą skubiai naudoti Pfizer ir BioNTech sukurtai vakcinai COVID-19.
- Naujienos pasirodė kitą dieną po to, kai FDA patariamasis komitetas rekomendavo agentūrai leisti vakciną
- Komiteto peržiūrėti duomenys parodė, kad vakcina yra veiksminga 95 proc.
- Vakcinos gali būti platinamos per 24 valandas nuo leidimo suteikimo.
Maisto ir vaistų administracija (FDA) penktadienio vakarą suteikė pirmosios vakcinos COVID-19 leidimą naudoti skubiai. Netrukus bus pradėta platinti „Pfizer Inc.“ ir Vokietijos bendrovės „BioNTech“ sukurta vakcina.
Ši naujiena sekė labai lauktą viešą klausymą ketvirtadienį, per kurį FDA patariamoji grupė balsavo 17–4 už „Pfizer“ vakcinos leidimą, vienam susilaikius.
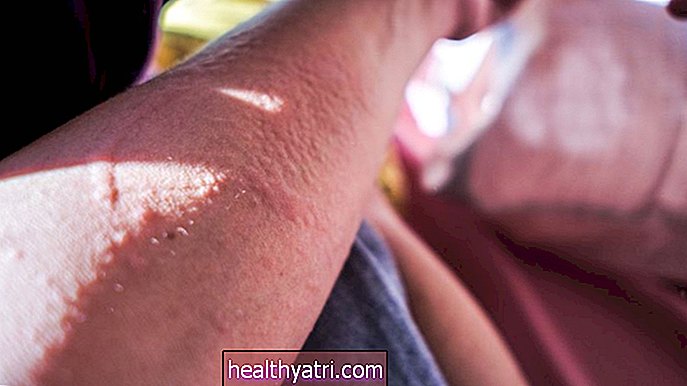
„Pfizer“ pateikė klinikinių tyrimų, kuriuose dalyvavo 43 000 suaugusių dalyvių, duomenis. Anksčiau šią savaitę FDA pasidalijo dalimi tų duomenų, įskaitant tai, kad 95% klinikiniame tyrime dalyvavusių žmonių, kurie gavo vakciną, nesukūrė COVID. -19. Šalutinis poveikis buvo nedidelis, įskaitant šaltkrėtimą, lengvą skausmą ir paraudimą injekcijos vietoje.
Skubaus naudojimo leidimas (EUA) taikomas 16 metų ir vyresniems žmonėms. „Pfizer“ taip pat atlieka klinikinius vakcinos saugumo ir veiksmingumo tyrimus jaunesniems kaip 12 metų vaikams ir tikimasi, kad papildys bandymus ir jaunesniems vaikams.
Vis dar reikia duomenų apie saugumą ir efektyvumą iš daugiau gyventojų
FDA patariamoji grupė, vadinama Vakcinų ir susijusių biologinių produktų konsultaciniu komitetu (VRBPAC), rekomenduoja „Pfizer“ imtis papildomų priemonių, kad jos vakcina būtų saugi ir veiksminga daugiau gyventojų. Ekspertų grupė pataria, kad į vykstančius klinikinius tyrimus būtų įtraukta daugiau spalvų žmonių. Spalvoti žmonės dažniau nei baltai užsikrėtė COVID-19 ir mirė nuo viruso.
Ekspertų grupė taip pat aptarė du alerginių reakcijų atvejus žmonėms, kurie šią savaitę vakcinavo JK, kur ji jau buvo patvirtinta. Filadelfijos vaikų ligoninės Vakcinų mokymo centro direktorius Paulas Offitas paklausė „Pfizer“ vedėjų apie alergines reakcijas, susirūpinęs, kad sunkią alergiją turintys žmonės gali nevartoti vakcinos. „Offit“ rekomendavo atlikti vakcinos tyrimus žmonėms, turintiems alergiją.
JK rekomenduoja žmonėms, turintiems anafilaksiją dėl vaisto ar maisto, negauti vakcinos. JAV gali pridėti panašų įspėjimą kartu su leidimu. FDA darbuotojai posėdyje komisijai sakė, kad jie jau rengia rašytinę dokumentaciją vartotojams apie vakcinos saugumą ir veiksmingumą.
Ką tai reiškia tau
Remdamasi patariamojo komiteto rekomendacija leisti naudoti Pfizer vakciną COVID-19, Maisto ir vaistų administracija galėjo patvirtinti jos vartojimą per kelias dienas. Po to platinimas galėtų prasidėti labai greitai.Tikimasi, kad pirmosios vakcinos dozės bus skiriamos sveikatos priežiūros darbuotojams ir slaugos namų gyventojams.
Po VRBPAC sprendimo FDA komisaras Stephenas M. Hahnas, MD, paskelbė pareiškimą:
„Paprastai dešimtims tūkstančių žmonių ištirtų vakcinų peržiūros procesas trunka mėnesius. Nors procesas buvo pagreitintas kartu su šios EUA peržiūra, FDA ekspertų peržiūros darbuotojai peržiūrėjo tūkstančius puslapių techninės informacijos [įskaitant] klinikinių tyrimų duomenis, neklinikinius duomenis apie vakcinos kūrimą laboratorijoje, ir gamybos duomenis apie vakcinos gamybą “.
Hahnas, greičiausiai siekdamas numalšinti vartotojų baimes, pridūrė: „Šiuo labai skubiu laikotarpiu FDA darbuotojai jaučia atsakomybę kuo greičiau pereiti per peržiūros procesą. Tačiau jie žino, kad privalo vykdyti savo įgaliojimus saugoti visuomenės sveikatą ir užtikrinti, kad bet kuri autorizuota vakcina atitiktų mūsų griežtus saugos ir veiksmingumo standartus, kurių tikėjosi Amerikos žmonės “.
Išrinktasis prezidentas Joe Bidenas po komiteto balsavimo taip pat paskelbė pareiškimą, kuriame sakoma: „mokslo vientisumas paskatino mus pasiekti šį tašką“.
FDA teigia, kad vakcinos gali būti platinamos per 24 valandas nuo leidimo suteikimo.
FDA patariamasis komitetas gruodžio 17 d., Ketvirtadienį, peržiūrės antrąją „Moderna“ pagamintą COVID-19 vakciną.








.jpg)