„Sasiistock“ / „Getty Images“
Pagrindiniai išsinešimai
- „Pfizer“ gavo FDA pritarimą pradėti koronaviruso vakcinos testavimą 12 metų ir vyresniems vaikams.
- Ekspertai teigia, kad vaikų įtraukimas į klinikinius tyrimus yra labai svarbus kuriant bendrą vakciną, kuri apsaugos vaikus ir suaugusiuosius nuo COVID-19.
- Anot savo svetainės, „Pfizer“ į savo tyrimą jau įtraukė daugiau nei 39 000 savanorių. Daugiau nei 34 000 tų savanorių jau yra paskiepyti antrą kartą.
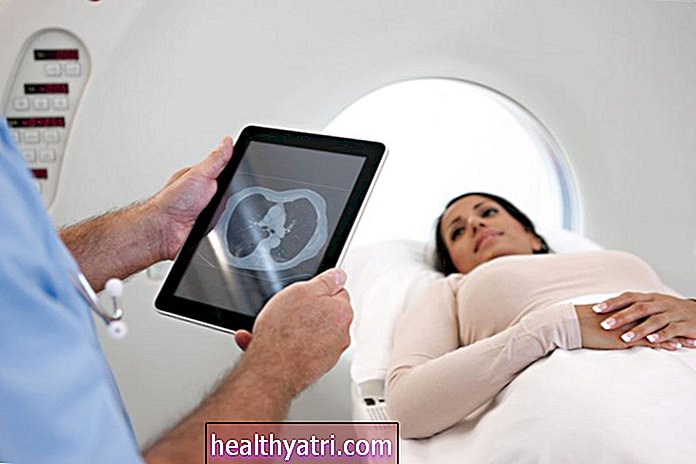
Jungtinių Valstijų farmacijos kompanija „Pfizer“ spalį paskelbė gavusi JAV maisto ir vaistų administracijos (FDA) leidimą pradėti registruoti 12 metų vaikus į koronaviruso vakcinos tyrimus.
„Tai darydami galėsime geriau suprasti galimą vakcinos saugumą ir veiksmingumą asmenims, turintiems daugiau amžiaus ir išsilavinimo“, - sakoma bendrovės atnaujintame pranešime.
Tai bus pirmasis COVID-19 vakcinos tyrimas JAV, kuriame dalyvaus vaikai. Nuo spalio mėnesio „Pfizer“ yra viena iš keturių JAV kompanijų, turinti vakcinų 3 fazės klinikinių tyrimų metu.
„Pfizer“ jau išplėtė 3 tyrimo etapą, įtraukdamas 16 metų ir vyresnius vaikus, taip pat žmones, sergančius lėtiniu, stabiliu žmogaus imunodeficito virusu (ŽIV), hepatitu C ir hepatitu B.
Kodėl reikia išbandyti COVID-19 vakciną vaikams?
Kol „Pfizer“ gavo patvirtinimą pradėti bandymus su vaikais, ekspertai žurnale paskelbė ataskaitąKlinikinės infekcinės ligosnurodant tokio testavimo svarbą.
"Tiesioginis COVID-19 poveikis vaikams yra didesnis nei pastebėtas daugeliui kitų patogenų, nuo kurių mes dabar turime veiksmingas vaikų vakcinas", - pažymima ataskaitoje. „Be to, akivaizdžiai neįvertintas vaikų vaidmuo perduodant SARS-CoV-2. Kruopščiai atlikti 2 fazės klinikiniai tyrimai gali tinkamai išspręsti galimas COVID-19 vakcinos saugumo problemas “.
Suzanne Pham, gyd
Mes negalime įveikti šio viruso plitimo, jei neskiepysime savo vaikų.
- Suzanne Pham, gydNiujorko Stony Brooko vaikų ligoninės Vaikų infekcinių ligų skyriaus vedėja Sharon Nachman sutinka su ataskaita, sakydama Verywell, kad „pediatrai yra labai suinteresuoti pamatyti išsamią tyrimo informaciją ir kaip vakcina veiks vaikams . “
Pasak Nachmano, yra tam tikrų privalumų išbandant vakciną vaikams. Tyrėjai galės įvertinti trumpalaikį ir ilgalaikį imuninį atsaką, įskaitant išsiaiškinimą, ar vakcinos dozė, naudojama suaugusiesiems, yra būtina vaikams, ar jie turėtų panašų imuninį atsaką į mažesnę dozę.
Nachmanas sako, kad taip pat svarbu atkreipti dėmesį į tai, kad prieš koronavirusą suaugusiesiems gali pasireikšti besimptomė vaikų infekcija, sukūrus vakciną visai šeimai gydyti, „būtų galima padaryti daug, kad sumažėtų perdavimas namuose ir bendruomenėje“.
Suzanne Pham, medicinos mokslų daktarė, Weisso memorialinės ligoninės, Čikagoje, vyriausioji medicinos pareigūnė, sako Verywell, kad kuo greičiau vaikai bus paskiepyti, tuo greičiau perdavimo greitis sumažės.
„Veiksmingai skiepijant vaikus, rizika, kad vaikai perduos virusą, sumažės, ypač tiems didelės rizikos žmonėms, kurie yra labiau linkę į sunkias ar kritines ligas“, - sako Phamas Verywellui. „Tai leis mokykloms vėl pradėti veikti ir kontroliuotai atnaujinti veiklą, reikalingą mūsų vaikų vystymuisi. Mes negalime įveikti šio viruso plitimo, jei neskiepysime savo vaikų. Mes turime turėti pakankamai bandos imuniteto visuomenėje, kad galėtume užkirsti kelią plitimui “.
„COVID-19“ vakcinos: sekite, kokios vakcinos yra, kas jas gali gauti ir kaip saugios.
Kaip prasideda vakcinos tyrimai?
Phamas paaiškina, kad norėdama išbandyti vakciną su suaugusiaisiais ar vaikais, įmonė pirmiausia turi pateikti FDA paraišką dėl naujų tyrimų (IND).
Paraiškoje bus aprašyta vakcina, kaip ji gaminama ir kokie kokybės kontrolės testai turi būti naudojami. Paraiškoje taip pat pateikiami bandymų su gyvūnais duomenys, kurie rodo, kad vakcina yra saugi pradiniams bandymams su žmonėmis.
Kaip paaiškina FDA, paraiškos teikimo procesas apima kelis veiksmus:
Ankstyvojo ikiklinikinio naujojo vaisto kūrimo metu rėmėjo pagrindinis tikslas yra nustatyti, ar produktas yra pakankamai saugus pradiniam vartojimui žmonėms ir ar šis junginys turi farmakologinį aktyvumą, kuris pateisina komercinį vystymąsi.
Kai produktas nustatomas kaip perspektyvus kandidatas tolesniam tobulinimui, rėmėjas sutelkia dėmesį į duomenų ir informacijos rinkimą, reikalingą tam, kad būtų nustatyta, jog produktas, naudojant ribotuose, ankstyvos stadijos klinikiniuose tyrimuose, nekels nepagrįstos rizikos.
Tada vakcinai bus atlikti 1 fazės bandymai, kurie Pham paaiškina: „saugumo ir imunogeniškumo tyrimai, atlikti nedaugeliui žmonių, kurie yra atidžiai stebimi“.
"2 etapas susideda iš dozių keitimo tyrimų ir yra išplėstas, įtraukiant didesnį skaičių žmonių (šimtus) žmonių", - sako Phamas. „Tada trečiojo etapo bandymai siekia įtraukti tūkstančius žmonių tiriamiesiems dokumentuoti efektyvumą ir toliau ieškoti saugos duomenų.“
Anot savo svetainės, „Pfizer“ į savo tyrimą įtraukė daugiau nei 39 000 savanorių. Daugiau nei 34 000 iš jų gavo antrą vakcinos dozę.
Ką tai reiškia tau
3 fazės klinikinis tyrimas, apimantis vaikų COVID-19 vakcinos testavimą, yra pažangos ženklas. Tačiau skiepytis negalima. Rezultatų galutiniam užbaigimui reikia laiko, kad apsaugotume tyrimo dalyvių, taip pat suaugusiųjų ir vaikų, kurie galiausiai gaus galutinę vakcinos versiją, saugumą.