Žmogaus imunodeficito virusas (ŽIV) yra retrovirusas, kurio genus vietoj dezoksiribonukleino rūgšties (DNR) koduoja ribonukleino rūgštis (RNR).
Retrovirusas skiriasi nuo tradicinio viruso tuo, kad jis užkrečia, dauginasi ir sukelia ligas.
ŽIV yra vienas iš tik dviejų savo klasės žmogaus retrovirusų, iš kurių kitas yra žmogaus T-limfotropinis virusas (HTLV).
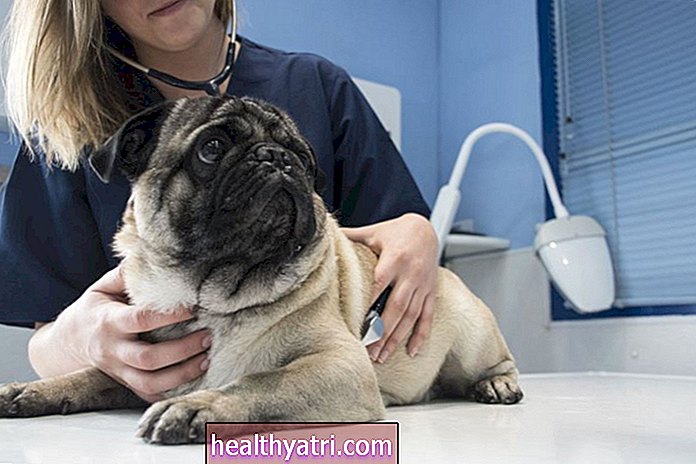
Thana Prasongsin / „Getty Images“
Kas yra retrovirusas?
ŽIV ir HTLV yra priskiriami IV šeimos RNR virusamsRetroviridae.Jie dirba įterpdami savo genetinę medžiagą į ląstelę, tada keičia savo genetinę struktūrą ir funkciją, kad galėtų pakartoti save.
ŽIV toliau klasifikuojamas kaip lentivirusas - retroviruso tipas, kuris jungiasi prie specifinio baltymo, vadinamo CD4.
Retroviridaevirusai galiužkrėsti žinduolius (įskaitant žmones) ir paukščius ir yra žinomi dėl to, kad sukelia imunodeficito sutrikimus, taip pat navikus.
Jų pagrindinė charakteristika yra fermentas, vadinamas atvirkštine transkriptaze, kuris perrašo RNR į DNR.
Daugeliu atvejų ląstelės paverčia DNR į RNR, kad ją būtų galima gaminti iš įvairių baltymų. Bet retrovirusuose šis procesas vyksta atvirkščiai (taigi „retro“ dalis), kai virusinė RNR virsta DNR.
Kaip užsikrečia ŽIV
ŽIV skiriasi nuo HTLV tuo, kad pastarasis yra deltaretrovirusas. Nors abiem būdinga atvirkštinė transkripcija, lentivirusai agresyviai replikuojasi, o deltaretrovirusai aktyviai dauginasi nustačius infekciją.
Tam, kad ŽIV užkrėstų kitas kūno ląsteles, jis išgyvena septynių pakopų gyvenimo (arba replikacijos) ciklą, todėl ląstelę šeimininkę paverčia ŽIV generuojančia gamykla. Štai kas nutinka:
- Susiejimas: radęs ir užpuolęs CD4 ląstelę, ŽIV prisijungia prie molekulių, esančių CD4 ląstelės paviršiuje.
- Susiliejimas: sujungus ląsteles, ŽIV viruso apvalkalas susilieja su CD4 ląstelių membrana, leidžiant ŽIV patekti į CD4 ląstelę.
- Atvirkštinė transkripcija: po to, kai ji patenka į CD4 ląstelę, ŽIV išsiskiria ir tada naudoja atvirkštinės transkriptazės fermentą, kad paverstų savo RNR į DNR.
- Integracija: Atvirkštinė transkripcija suteikia ŽIV galimybę patekti į CD4 ląstelės branduolį, kur patekęs į vidų išskiria kitą fermentą, vadinamą integraze, kurį jis naudoja savo viruso DNR įterpti į ląstelės-šeimininkės DNR.
- Replikacija: Dabar, kai ŽIV yra integruotas į priimančiosios CD4 ląstelės DNR, jis pradeda naudoti jau CD4 ląstelės viduje esančias mašinas, kad sukurtų ilgas baltymų grandines, kurios yra pagrindas daugiau ŽIV.
- Surinkimas: Dabar naujos ŽIV RNR ir ŽIV baltymai, kuriuos gamina CD4 ląstelė-šeimininkė, pereina į ląstelės paviršių ir formuoja nesubrendusį (neinfekcinį) ŽIV.
- Pradinis: Šis nesubrendęs ŽIV, kuris negali užkrėsti kitos CD4 ląstelės, verčiasi išeiti iš šeimininko CD4 ląstelės. Ten jis išskiria dar vieną ŽIV fermentą, vadinamą proteaze, kuris suardo nesubrendusio viruso ilgąsias baltymų grandines. Tai darydamas, jis sukuria brandų - ir dabar infekcinį - virusą, kuris dabar yra pasirengęs užkrėsti kitas CD4 ląsteles.
Terapijos tikslai
Suprasdami aukščiau aprašytus replikacijos mechanizmus, mokslininkai gali nukreipti ir blokuoti tam tikrus ŽIV gyvenimo ciklo etapus.
Sutrikus jo gebėjimui daugintis, viruso populiacija gali būti nuslopinta iki neaptinkamo lygio, o tai yra ŽIV antiretrovirusinių vaistų tikslas.
Šiuo metu ŽIV gydymui yra devynios skirtingos antiretrovirusinių vaistų grupės, suskirstytos pagal jų blokuojamo gyvenimo ciklo stadiją:
Įvažiavimo / priedų inhibitorius
Ką jie daro: Prisiriša prie baltymų ant išorinio ŽIV paviršiaus, neleisdami ŽIV patekti į CD4 ląsteles.
Šios klasės vaistas (-ai): Fostemsaviras
Po prisirišimo inhibitorius
Ką jie daro: blokuokite CD4 receptorius tam tikrų imuninių ląstelių paviršiuje, kurių ŽIV turi patekti į ląsteles.
Šios klasės vaistas (-ai): Ibalizumab-uiyk
Sintezės inhibitorius
Ką jie daro: Užblokuokite ŽIV patekimą į imuninės sistemos CD4 ląsteles.
Šios klasės vaistas (-ai): Enfuvirtide
CCR5 antagonistai
Ką jie daro: blokuokite CCR5 koreceptorius tam tikrų imuninių ląstelių paviršiuje, kurių ŽIV turi patekti į ląsteles.
Šios klasės vaistai (-ai): maravirokas
Nukleozidų atvirkštinės transkriptazės inhibitoriai (NRTI)
Ką jie daro: Blokuokite atvirkštinę transkriptazę. ŽIV fermentas turi pasidaryti savo kopijas.
Šios klasės vaistai (-ai): abakaviras, emtricitabinas, lamivudinas, tenofoviro dizoproksilio fumaratas, zidovudinas
Nukleozidų atvirkštinės transkriptazės inhibitoriai (NNRTI)
Ką jie daro: Prisiriša ir vėliau keičia atvirkštinę transkriptazę. ŽIV fermentas turi pasidaryti savo kopijas.
Šios klasės vaistai (-ai): Doravirinas, efavirenzas, etravirinas, nevirapinas, rilpivirinas
Proteazių inhibitoriai (PI)
Ką jie daro: blokuoja ŽIV proteazę. ŽIV fermentas turi pasidaryti savo kopijas.
Šios klasės vaistai (-ai): atazanaviras, darunaviras, fosamprenaviras, ritonaviras, sakvinaviras, tipranaviras
„Integrase Strand Transfer Inhibitor“ (INSTI)
Ką jie daro: blokuoja ŽIV integrazę. ŽIV fermentas turi pasidaryti savo kopijas.
Šios klasės vaistai (-ai): kabotegraviras, dolutegraviras, raltegraviras
Farmakokinetikos stiprikliai (stiprintuvai)
Ką jie daro: vartojami gydant ŽIV, siekiant padidinti ŽIV gydymo į ŽIV režimą veiksmingumą.
Šios klasės vaistas (-ai): kobicistatas
Kodėl nėra vieno antiretrovirusinio vaisto, galinčio viską padaryti?
Dėl didelio genetinio ŽIV kintamumo, derinant antiretrovirusinį gydymą reikia blokuoti įvairius gyvenimo ciklo etapus ir užtikrinti ilgalaikį slopinimą. Iki šiol nė vienas antiretrovirusinis vaistas to padaryti negali.
Iššūkiai ir tikslai
Lentivirusai dauginasi agresyviai - ūminės infekcijos metu padvigubėja 0,65 dienos, tačiau tas replikacijos procesas yra linkęs į klaidas. Tai reiškia didelį mutacijos dažnį, kurio metu asmeniui per vieną dieną gali išsivystyti keli ŽIV variantai.
Daugelis šių variantų yra negyvybingi ir negali išgyventi. Kiti yra perspektyvūs ir kelia iššūkių gydymui ir vakcinų kūrimui.
Atsparumas vaistams
Vienas reikšmingas iššūkis veiksmingai gydyti ŽIV yra viruso gebėjimas mutuoti ir daugintis, kol žmogus vartoja antiretrovirusinius vaistus.
Tai vadinama ŽIV atsparumu vaistams (ŽIVDR) ir tai gali pakenkti dabartinių terapinių galimybių veiksmingumui ir tikslui sumažinti ŽIV paplitimą, mirtingumą ir sergamumą.
Laukinio tipo ŽIV
ŽIV atsparumas vaistams gali išsivystyti dėl vadinamojo „laukinio tipo“ ŽIV, kuris yra vyraujantis neapdoroto viruso telkinio variantas, dėl to, kad jis gali išgyventi, kai kiti variantai to negali.
Virusinė populiacija gali pradėti keistis tik tada, kai žmogus pradeda vartoti antiretrovirusinius vaistus.
Kadangi negydytas ŽIV taip greitai replikuojasi ir dažnai apima mutacijas, gali būti, kad gali susidaryti mutacija, galinti užkrėsti ląsteles šeimininkes ir išgyventi, net jei asmuo vartoja antiretrovirusinius vaistus.
Taip pat gali būti, kad vaistams atspari mutacija tampa dominuojančiu variantu ir dauginasi. Be to, atsparumas gali išsivystyti dėl blogo gydymo laikymosi, dėl kurio gali pasireikšti daugkartinis atsparumas vaistams ir nesėkmingas gydymas.
Kartais, kai žmonės yra naujai užsikrėtę ŽIV, jie paveldi atsparų viruso štamą iš juos užkrėtusio asmens - tai vadinama perduotu atsparumu. Netgi kažkas naujai užsikrėtęs gali paveldėti gilų, daugelio vaistų atsparumą kelioms ŽIV vaistų klasėms.
Naujesni ŽIV gydymo būdai suteikia daugiau apsaugos nuo mutacijų
Kai kai kuriems senesniems ŽIV vaistams, tokiems kaip Viramune (nevirapinas) ir Sustiva (efavirenzas), gali pasireikšti atsparumas ŽIV tik su viena mutacija, naujesniems vaistams prieš gedimą reikia daugybės mutacijų.
Vakcinų kūrimas
Viena iš reikšmingiausių kliūčių kuriant plačiai veiksmingą ŽIV vakciną yra paties viruso genetinė įvairovė ir kintamumas. Užuot sugebėję sutelkti dėmesį į vieną ŽIV atmainą, mokslininkai turi atsižvelgti į tai, kad ji taip greitai dauginasi.
ŽIV replikacijos ciklas
ŽIV replikacijos ciklas trunka šiek tiek daugiau nei 24 valandas.
Nors dauginimosi procesas yra greitas, jis nėra pats tiksliausias - kiekvieną kartą sukuriama daugybė mutavusių kopijų, kurios sujungiamos ir sukuria naujas padermes, nes virusas perduodamas tarp skirtingų žmonių.
Pavyzdžiui, ŽIV-1 (viena ŽIV atmaina) yra 13 skirtingų porūšių ir potipių, kurie yra susieti geografiškai, 15–20% porūšio pokyčiai ir iki 35% potipių skirtumai.
Tai ne tik iššūkis kuriant vakciną, bet ir todėl, kad kai kurios mutavusios padermės yra atsparios ART, o tai reiškia, kad kai kurie žmonės turi agresyvesnes viruso mutacijas.
Kitas iššūkis kuriant vakciną yra kažkas, vadinamas latentiniais rezervuarais, kurie įsitvirtina ankstyviausioje ŽIV infekcijos stadijoje ir gali veiksmingai „paslėpti“ virusą nuo imuninio aptikimo, taip pat nuo ART poveikio.
Tai reiškia, kad jei gydymas kada nors bus nutrauktas, latentiškai užkrėstą ląstelę galima vėl suaktyvinti, todėl ląstelė vėl pradės gaminti ŽIV.
Nors ART gali slopinti ŽIV lygį, jis negali pašalinti latentinių ŽIV rezervuarų - tai reiškia, kad ART negali išgydyti ŽIV infekcijos.
Latentinių ŽIV rezervuarų iššūkiai
Kol mokslininkai nesugebės „išvalyti“ latentinių ŽIV rezervuarų, mažai tikėtina, kad kokia nors vakcina ar terapinis būdas virusą išnaikins iki galo.
Taip pat yra iššūkis dėl imuninio išsekimo, atsirandančio dėl ilgalaikės ŽIV infekcijos. Tai laipsniškas imuninės sistemos gebėjimo atpažinti virusą ir pradėti tinkamą atsaką praradimas.
Bet kokio tipo ŽIV vakcina, gydymas nuo AIDS ar kitas gydymas turi būti sukurtas atsižvelgiant į imuninės sistemos išsekimą, ieškant būdų, kaip spręsti ir kompensuoti silpstančius žmogaus imuninės sistemos pajėgumus laikui bėgant.
ŽIV vakcinos tyrimų pažanga
Tačiau vakcinos tyrimuose padaryta tam tikra pažanga, įskaitant eksperimentinę strategiją, vadinamą „spardyk ir nužudyk“. Tikimasi, kad latentą pakeičiančio agento ir vakcinos (ar kitų sterilizuojančių medžiagų) derinys gali būti sėkmingas taikant gydomąją, eksperimentinę strategiją, vadinamą „spardyk ir nužudyk“ (dar žinomas kaip „smūgis ir žudymas“).
Iš esmės tai yra dviejų etapų procesas:
- Pirma, vaistai, vadinami latentą pakeičiančiais agentais, naudojami imuninės ląstelėse pasislėpusio latentinio ŽIV aktyvavimui („smūgio“ ar „šoko“ dalis).
- Tada, kai imuninės ląstelės bus vėl suaktyvintos, organizmo imuninė sistema arba vaistai nuo ŽIV gali nukreipti ir užmušti reaktyvuotas ląsteles.
Deja, vien latentą keičiantys agentai negali sumažinti viruso rezervuarų dydžio.
Be to, kai kurie iš perspektyviausių vakcinos modelių iki šiol apima plačiai neutralizuojančius antikūnus (bNAbs) - retą antikūnų tipą, kuris gali nukreipti daugumą ŽIV variantų.
BNAbs pirmą kartą buvo atrasti keliuose ŽIV elito kontrolieriuose - žmonėms, kurie, atrodo, turi galimybę slopinti viruso replikaciją be ART ir nerodo jokių ligos progresavimo požymių. Kai kurie iš šių specializuotų antikūnų, pavyzdžiui, VRC01, gali neutralizuoti daugiau nei 95% ŽIV variantų.
Šiuo metu vakcinų tyrėjai bando skatinti bNAb gamybą.
2019 m. Tyrimas, kuriame dalyvavo beždžionės, rodo pažadą. Gavę vieną ŽIV vakcinos šūvį, šeši iš 12 bandymo beždžionių sukūrė antikūnus, kurie žymiai atitolino infekciją ir - dviem atvejais - netgi užkirto kelią.
Šis požiūris vis dar yra ankstyvoje bandymų su žmonėmis stadijoje, nors 2020 m. Kovo mėn. Buvo paskelbta, kad mokslininkai pirmą kartą sugebėjo sukurti vakciną, kuri paskatino žmogaus ląsteles generuoti bNAbs.
Tai yra reikšmingas įvykis praėjus keleriems metams po ankstesnių tyrimų, kuriuos iki šio momento stabdo tvirto ar specifinio bNAb atsako nebuvimas.
ŽIV vektoriai genų terapijoje
Inaktyvuota ŽIV dabar tiriama kaip galima pristatymo sistema, skirta gydyti kitas ligas, įskaitant:
- Leukemija
- Sunkus kombinuotas imunodeficitas (SCID)
- Metachromatinė leukodistrofija
Paversdami ŽIV neinfekciniu „vektoriu“, mokslininkai mano, kad jie gali panaudoti virusą genetiniam kodavimui perduoti ląstelėms, kurias ŽIV pirmenybiškai infekuoja.
Žodis iš „Wellwell“
Geriau suprasdami retrovirusų veikimo būdą, mokslininkai sugebėjo sukurti naujus vaistus.
Nepaisant to, kad dabar yra gydymo būdų, kurių anksčiau nebuvo, geriausia žmogaus galimybė gyventi ilgą ir sveiką gyvenimą su ŽIV pasireiškia diagnozuojant kuo anksčiau, atliekant reguliarius tyrimus.
Ankstyva diagnozė reiškia ankstesnį gydymą - jau nekalbant apie su ŽIV susijusių ligų sumažėjimą ir gyvenimo trukmės padidėjimą.
















.jpg)

-and-asthma.jpg)